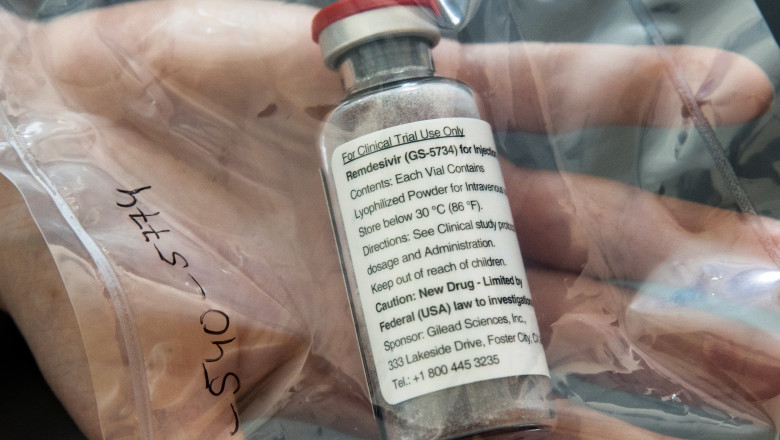
Agenția Europeană pentru Medicamente a început procesul de evaluare a Remdesivir, medicamentul care a avut rezultate pozitive în tratamentul pacienților infectați cu noul tip de coronavirus, în SUA, anunță europarlamentarul Cristian Bușoi.
„Revizuirea continuă” începută de agenția europeană este unul dintre instrumentele de reglementare care permite Agenției evaluarea rapidă a unui medicament promițător în timpul urgențelor de sănătate publică, așa cum este pandemia de coronavirus, explică europarlamentarul într-un comunicat citat de Mediafax.
Agenția va evalua toate datele privind acest medicament, inclusiv probe dintr-un studiu recent publicat în China pentru a evalua, cât mai curând posibil, beneficiile medicamentului, dar și riscurile care pot interveni la administrarea acestuia.
„În calitate de responsabil al Comisiei pentru Sănătate Publică, ENVI, și Parlamentului European în relația cu Agenția Europeană pentru Medicamente, sunt în permanent contact cu conducerea Agenției și am insistat pentru accelerarea tuturor procedurilor pentru a răspunde rapid provocărilor crizei coronavirus. Deși Remdesivir nu este încă autorizat în Uniunea Europeană, acesta este disponibil, inclusiv în România, pentru pacienți prin studii clinice și așa-numitele programe de <utilizare compasivă>, prin care bolnavii pot avea acces la medicamente neautorizate în situații de urgență”, spune Bușoi.
În Statele Unite, rezultatele preliminare ale unui studiu făcut de guvern au arătat că pacienții cărora li s-a administrat Remdesivir s-au vindecat cu 31% mai repede decât cei care au primit tratament placebo. Aceste date au fost apreciate de medicul Anthony Fauci, expertul de vârf al SUA în bolile infecțioase, ca „foarte semnificative”.
„Dacă procedurile de la nivelul UE se vor desfășura în mod accelerat, așa cum a anunțat deja Agenția Europeană pentru Medicamente, pacienții europeni vor putea beneficia de acest tratament la timp”, a spus europarlamentarul.